 UDI一站式服务平台
UDI一站式服务平台
对于医疗器械生产企业而言,实施UDI的第一步,就是要了解和选择发码机构。
我国药监局认可的UDI发码机构仅有三家,分别是中国物品编码中心、中关村工信二维码技术研究院和阿里健康科技(中国)有限公司。
中国物品编码中心发行的代码为GS1码;中关村工信二维码技术研究院发行的代码为MA码;阿里健康科技(中国)有限公司发行的代码为AHM码。
目前,GS1码在医疗器械唯一标识市场中占据主导地位,MA码次之,AHM码可以忽略不计。今天,我们重点分析GS1和MA这两种编码体系编制的UDI有何不同。
▍GS1编码体系
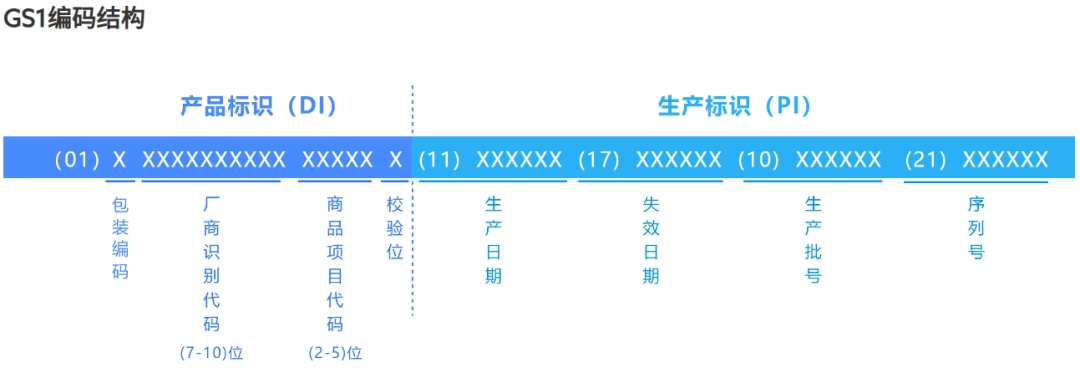
基于GS1标准的UDI码,产品标识(DI)由包装指示符、厂商识别代码、商品项目代码、校验码四部分组成,数据类型为数字,数据长度为14位。
厂商识别代码:7-10位数字,由中国物品编码中心负责分配和管理。厂商识别代码的前3位代码为前缀码,国际物品编码组织分配给中国物品编码中心的前缀码为690-699。
项目代码:2-5位数字,由医疗器械注册人/备案人根据相应编码原则编制。
校验码:1位数字,用于检验译码正确性。算法详见GB 12904《商品条码 零售商品编码与条码表示》附录B,也可以通过UDI一站式服务平台自动生成。
包装指示符:1位数字,取值范围是0-9,表示产品的不同包装级别。
产品标识(PI)由应用标识符(AI)及其对应的编码表示,信息内容可根据监管以及实际需求进行选择,如生产日期、有效期、批次号等等。
GS1编码规则:
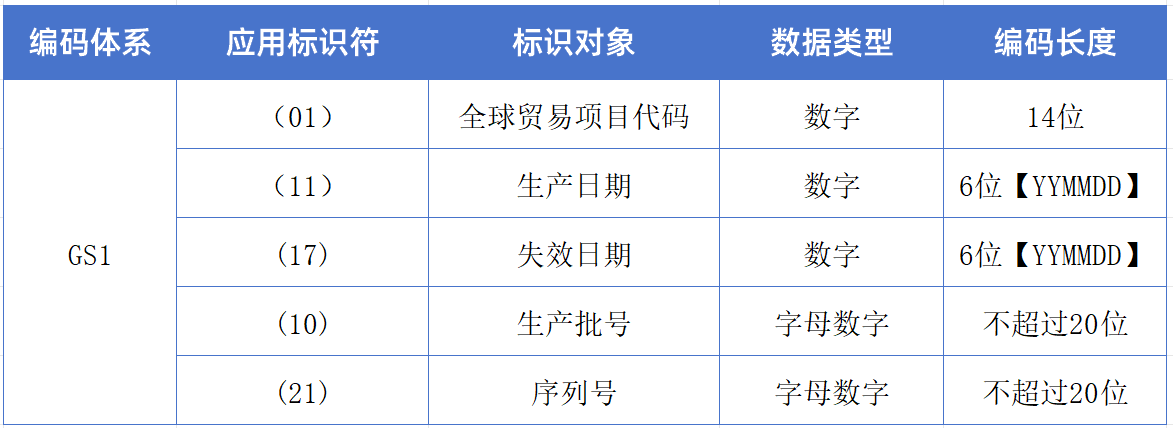
▍MA编码体系
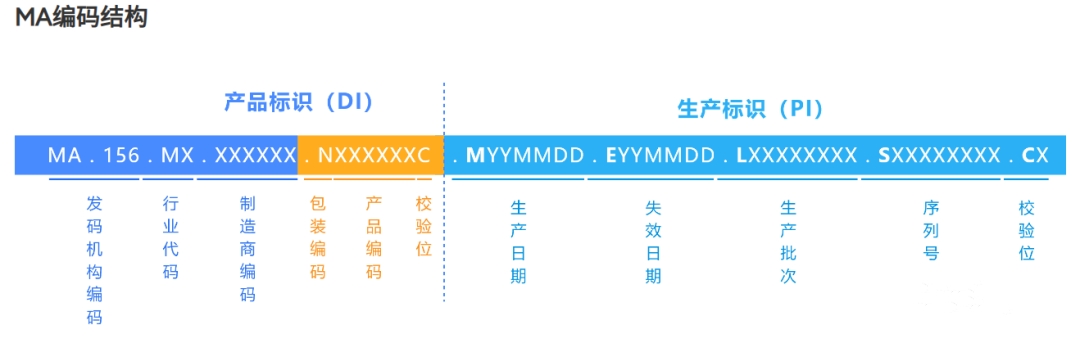
基于MA标准的UDI码,产品标识由发码机构编码、行业代码、制造商编码、包装编码、产品编码、校验位组成。前三个部分由ZIIOT负责分配,后三个部分由生产厂商自行分配,用于标识产品的具体型号或规格等信息。数据类型为字符数字,数据长度为25位。
产品标识(PI)由生产厂商根据生产情况动态分配,一般包含序列号、生产批号、生产日期、失效日期等。
MA编码规则:
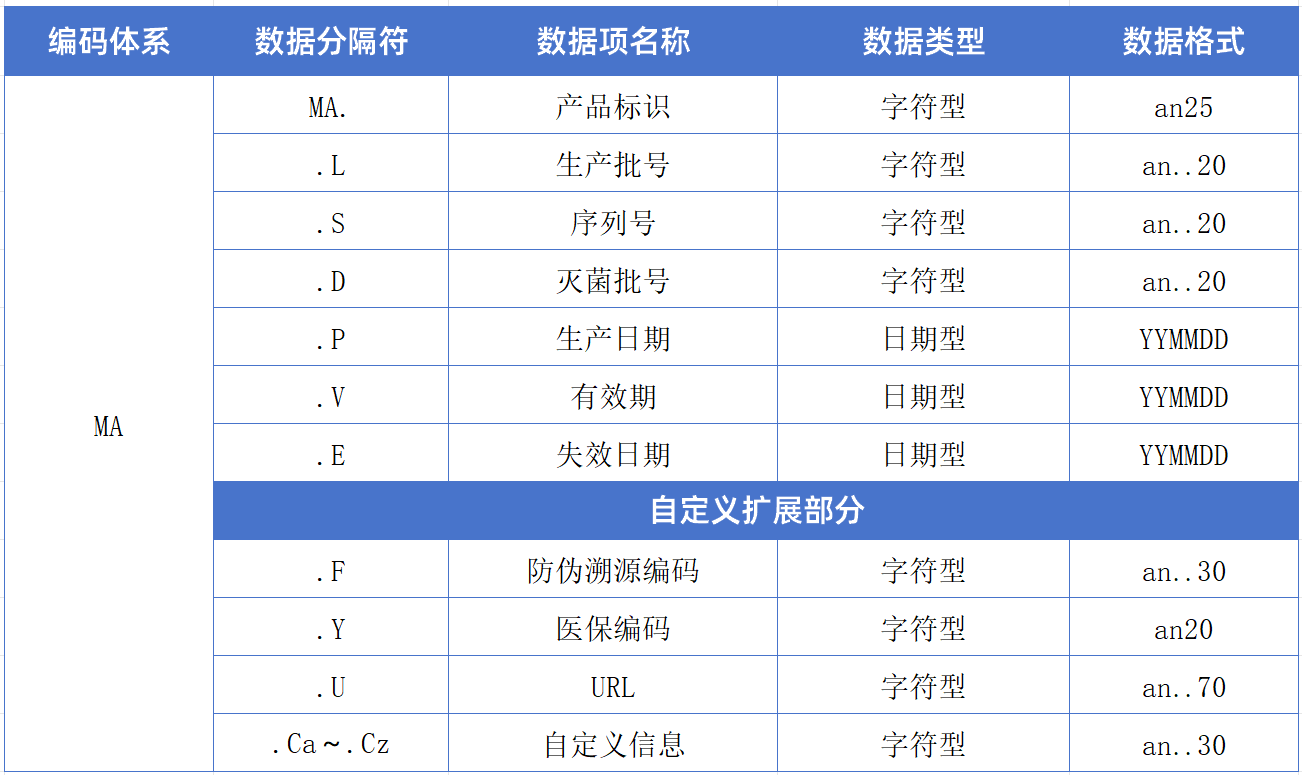
数据格式中字符的含义:

编码体系怎么选 ?
企业在选择编码体系时,需要综合考虑产品的行销范围、下游医疗机构的需求、发码机构配套服务等。
GS1和MA均符合国家药监局的要求,不过它们在设计、应用和特点上存在一些差异。综合来说,我们更推荐企业使用GS1标准,主要有以下原因:
1、国际认可度
GS1标准已得到美国、欧盟、日本、韩国等众多国家和地区的认可,满足目前全球所有已发布的UDI相关规定,流通范围更广,MA主要应用于国内。所以企业产品涉及出口业务时,须选择GS1编码体系。
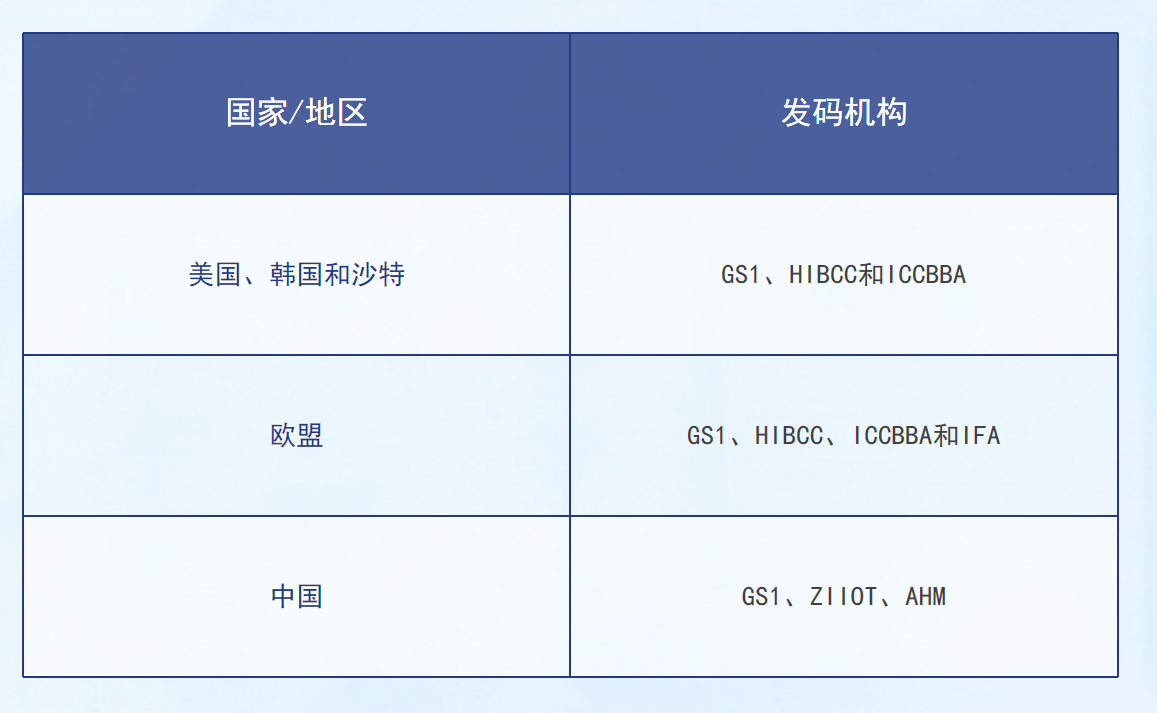
△GS1是唯一同时满足中美欧UDI要求的标准体系
2、落地体系完善
GS1在全球有100多个成员组织,在国内设置了47家物品编码分支机构,可以更好地解决企业的实际应用问题。
3、下游UDI码识读
GS1码在医疗器械领域已应用多年,医疗器械经营企业、医疗机构的相关系统和设备都能支持GS1码的扫码和解析,不会有识读阻碍。
MA码在医疗器械行业推行的时间相对较短,部分企业和机构的相关系统和设备可能不支持解析MA码。这个时候,需要生产企业去与下游机构沟通,是否能改造系统,从而达到识读MA码的目的。这样无疑会加大生产企业与下游机构的工作量。
4、追溯系统的兼容性
目前,部分省市的药监平台已陆续上线UDI追溯系统。有些省市的追溯系统,MA码可能不兼容,这就会导致相关企业需要将MA码换成GS1码,重新赋码,使得实施成本和实施时间增加。
5、PI扩展性
GS1标准下,除了生产日期、失效日期这几个常规的标识符,还有100多个标识符可以作为PI的组成,扩展性更强。
6、标准完善
GS1-128、GS1 Data Matrix码在质检和配色等方面有着完善的标准,可以提升企业实操效率。
7、企业使用率
根据官方数据,目前国家药监局UDI数据库内应用GS1标准的企业,占比已超过93%,其余两种编码体系加起来不到10%,GS1占据着绝对主导地位。
8、示范单位应用
此前国家药监局综合司公布的首批15家医疗器械唯一标识示范单位,7家生产企业,2家经营企业,6家医疗机构,全部应用的GS1标准。

公众号
研发中心
长沙高新区麓谷企业广场F3栋10楼
运营中心
长沙雨花区双塔国际广场B座14楼
南京办事处
南京栖霞区红枫科技园D11栋6楼
联系方式
400 900 3068
商务邮箱
market@rzdata.net
客服邮箱
support@rzdata.net


