 UDI一站式服务平台
UDI一站式服务平台
细心的朋友可以发现,有些医疗器械产品的包装上会同时存在两种条形码:商品条码和UDI码。有的企业可能存在疑惑,一个产品为何要应用两种编码,它们之间能相互替代吗?
部分人对商品条码和UDI码的概念还比较模糊,容易混淆。为了便于大家理解和区分,我们可以从以下6个方面来分析这两种条码:
1 定义不同
《商品条码零售商品编码与条码表示》(GB12904-2008)中对于商品条码的定义: 是由一组规则排列的条、空及其对应代码组成,表示商品代码的条码符号,包括零售商品、储运包装商品、物流单元、参与方位置等等的代码与条码标识。
《医疗器械唯一标识系统规则》中对于UDI码的定义:是指在医疗器械产品或者包装上附载的,由数字、字母或者符号组成的代码,用于对医疗器械进行唯一性识别。
2 应用范围不同
商品条码广泛应用于商品零售、物流管理、医疗卫生、电子商务、食品追溯、政府采购等领域。
UDI码是医疗器械产品的专属“身份证”,仅应用在医疗器械领域。
3 实施对象不同
商品条码:依法取得营业执照和相关合法经营资质证明的生产者、销售者和服务提供者可申请注册厂商识别代码,然后编制商品条码并备案使用。
UDI码:由医疗器械注册人、备案人按照规则创建和维护。
4 代码结构不同
GTIN共四种不同的代码结构:非零售商品标识代码GTIN-14、零售商品标识代码GTIN-13(原称EAN-13)、零售商品标识代码GTIN-12(原称UPC-12)、零售商品标识代码GTIN-8(原称EAN-8)。
商品条码:

△商品条码
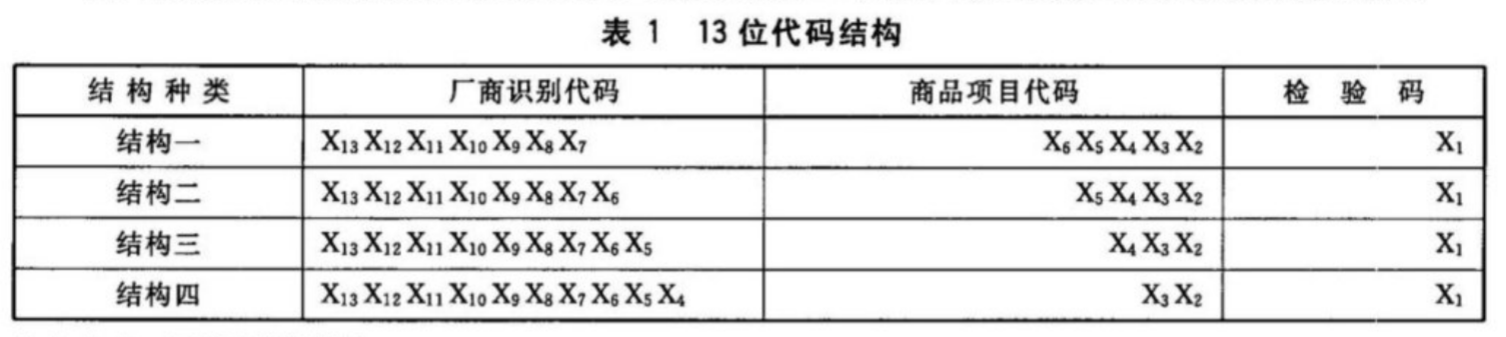
我国零售领域的商品条码最常见的是GTIN-13,由厂商识别代码、商品项目代码、校验码三个部分组成,代码结构如下:
UDI码:

△UDI一维条码(非正式码)
医疗器械唯一标识由产品标识(DI)和生产标识(PI)组成。
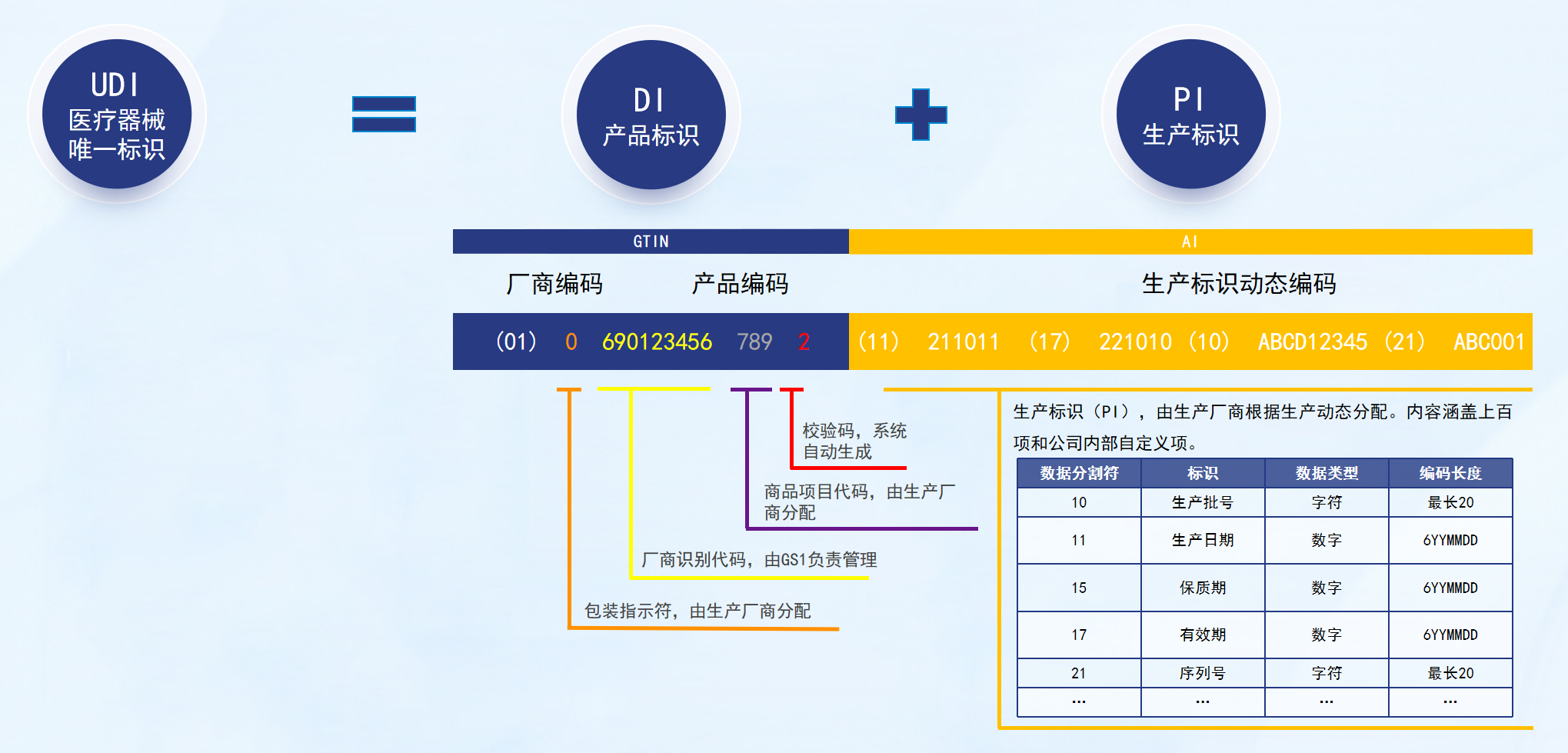
以GS1码制为例,UDI-DI采用的GTIN-14,由包装指示符、厂商识别代码、商品项目代码、校验码四个部分组成。
UDI-PI由生产过程中的动态数据组成,生产厂商可根据监管和实际应用需求,确定将生产批号、生产日期、失效日期、序列号等作为PI组成部分,结构不固定。
5 应用价值不同
商品条码:
在生产环节使用商品条码,可以便于企业进行生产管理,提高生产效率,节约流通、存储、人工等方面的成本。分销商使用商品条码进行商品的运输和存储,可以及时了解商品销售情况,更好地管理库存,降低经营成本。零售环节使用商品条码可以让商家轻松地识别和管理商品,提升结算速度,为消费者提供更加便捷、安全的消费体验。
UDI码:
医疗器械行业关乎人的生命健康安全,我国对医疗器械行业实行严格的监督管理制度。建立医疗器械唯一标识系统,有利于实现监管数据的整合和共享,提升监管效能,加强医疗器械全生命周期管理,净化市场、优化营商环境。
对于医疗器械生产企业,利用UDI有助于提升企业信息化管理水平,建立产品追溯体系,加强行业自律,提升企业管理效能,助推医疗器械产业高质量发展。对于医疗器械经营企业,利用UDI,可建立符合现代化的物流体系,实现医疗器械供应链的透明化、可视化、智能化。对于医疗机构,利用UDI,有利于减少用械差错,提升院内耗材管理水平,维护患者安全。
6 实施要求不同
商品条码:
《商品条码管理办法》第二十二条规定:销售者应当积极采用商品条码。销售者在其经销的商品没有使用商品条码的情况下,可以使用店内条码。店内条码的使用,应当符合国家标准《店内条码》(GB/T18283)的有关规定。也就是说,企业使用商品条码是自愿而非强制。
但要注意的是,任何单位和个人未经核准注册不得使用厂商识别代码和相应的条码。任何单位和个人不得在商品包装上使用其他条码冒充商品条码;不得伪造商品条码,否则涉嫌违法。
UDI码:
从2021年开始,我国采用分步实施的方式对医疗器械强制施行UDI制度:
2021年1月1日,9大类69种第三类医疗器械要求实施UDI。
2022年6月1日,其他第三类医疗器械(含体外诊断试剂)纳入UDI实施产品名录。
2024年6月1日,共15大类103种第二类医疗器械增设为UDI实施产品,包括部分临床需求量较大的一次性使用产品、集中带量采购中选产品、医疗美容相关产品等。
未按要求实施UDI的企业,《医疗器械生产监督管理办法》明确了相关处罚措施,最高可处5万元以上10万元以下罚款。
总之,商品条码和UDI码在不同的领域发挥着重要作用,二者不可相互替代。由于UDI码有着强政策推动性,还未正式实施UDI的医疗器械企业应抓紧时间合规赋码,以应对药监等部门的抽查、巡检,确保产品顺利流通。

公众号
研发中心
长沙高新区麓谷企业广场F3栋10楼
运营中心
长沙雨花区双塔国际广场B座14楼
南京办事处
南京栖霞区红枫科技园D11栋6楼
联系方式
400 900 3068
商务邮箱
market@rzdata.net
客服邮箱
support@rzdata.net


