 UDI一站式服务平台
UDI一站式服务平台
一份紧急通报,揭露了医疗器械行业的质量管理体系隐忧,是时候拥抱智能化文控系统的变革浪潮了。
国家药监局核查中心于2025年11月28日发布本年度第三批医疗器械飞行检查情况通告。通报显示,34家医疗器械生产企业的质量管理体系存在不符合《医疗器械生产质量管理规范》的相关问题。
本次飞行检查覆盖范围广、针对性强,再次对行业敲响警钟:质量管理体系的规范运行是保障医疗器械安全有效的生命线,任何环节的疏漏都可能引发严重的合规风险。
通告责令相关省药监局督促企业整改,并要求企业对存在安全风险的产品主动召回。
这表明,监管态势日趋严格,事后整改与召回不仅带来巨大的经济损失,更将严重损害企业声誉与市场信任。
01-飞检之痛,文件管理风险高悬
根据本次通报中详细披露的每家企业的具体缺陷项,并结合2025年第一批、第二批飞检报告及行业长期存在的问题来看,“文件管理混乱”始终是飞检不符合项的“重灾区”。
文件是质量体系运行的载体和证据,文件管理的失控,直接意味着质量管理体系的失效。这些问题通常表现为:
文件控制体系失灵:
文件编号规则不一,版本更新不及时,新旧版本并存现场,作废文件未有效回收隔离,导致错误版本文件被误用。
记录管理流于形式:
关键生产、检验记录填写不规范、不完整,甚至缺失;记录修改未按规定划改签注,追溯性无从谈起。
外来文件与法规更新脱节:
未建立有效渠道识别、获取并转化最新法规、标准和技术文件,导致实际运作与现行要求脱节。
设计开发文档管理缺失:
设计变更记录不完整,验证确认文档缺失,无法证明产品设计输出的充分性与安全性。
这些问题背后,暴露的是企业文件管理依赖人工、流程割裂、信息孤岛的传统管理模式已难堪重负。面对海量文件、频繁变更和严格的追溯要求,人工管理不仅效率低下,更极易出错,为企业的合规运营埋下深水炸弹。
为何文件管理问题屡查屡犯,成为众多企业的顽疾?其根源在于传统管理方式存在难以克服的系统性缺陷。
纸质与电子表格(Excel)混合的“双轨制”,是混乱之源。文件分发靠打印、签收靠手写、回收靠催要、台账靠Excel更新。这种模式导致:
信息不同步:
电子版已更新至V3.0,现场可能还在使用V2.0的纸质文件。
追溯如大海捞针:
当发生偏差或需要审计时,查找一份文件的所有历史版本、分发记录、签收人员,需要翻遍档案柜和多个Excel表格,耗时耗力且难以保证准确性。
效率极其低下:
从文件修订申请、跨部门会签、批准发布到培训生效,流程漫长,严重拖慢产品改进和问题响应的速度。
安全风险突出:
敏感技术文件、工艺图纸可能通过邮件、U盘随意传播,或滞留在离职员工电脑中,存在泄露风险。
这些痛点清晰表明,依靠零散工具和人工纪律已无法满足现代医疗器械企业对于文件“准确性、及时性、可追溯性”的刚性合规要求。企业亟需一套系统性、一体化、智能化的文件管理解决方案。
03-破局之道:构建全生命周期智能文控体系
解决飞检中暴露的文件管理问题,不能仅停留在“头痛医头、脚痛医脚”的局部整改,而需要进行顶层设计和管理模式的数字化转型。
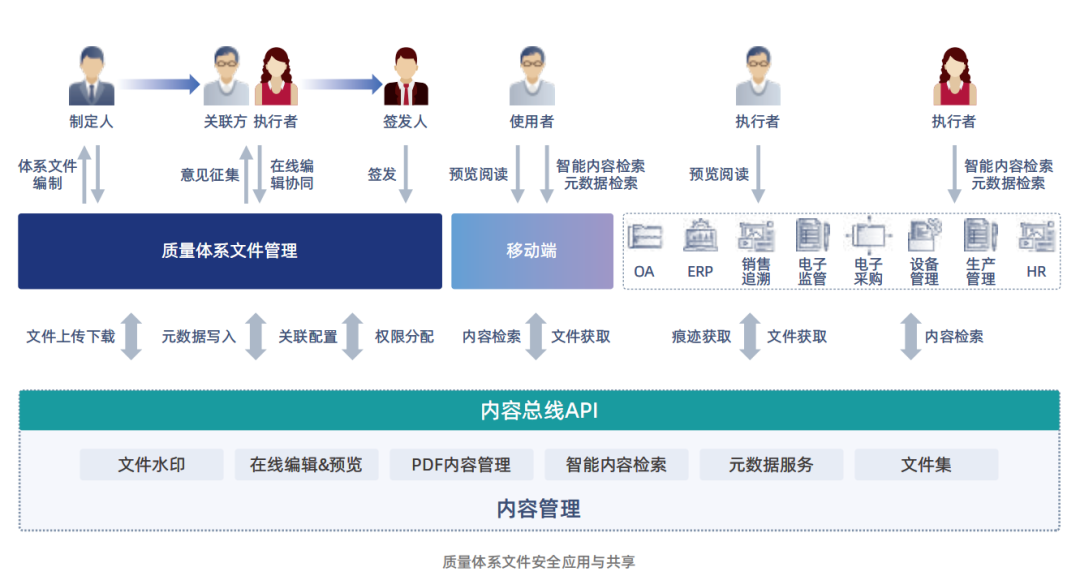
睿展数据DMS体系文件管理系统,正是为破解这一行业共性难题而生。系统严格遵循NMPA、FDA、GMP、ISO13485等国内外医疗器械法规与质量标准,将文件管理的全生命周期置于一个统一、受控、智能、可追溯的数字化平台上。
核心解决场景一:杜绝“编号与版本混乱”
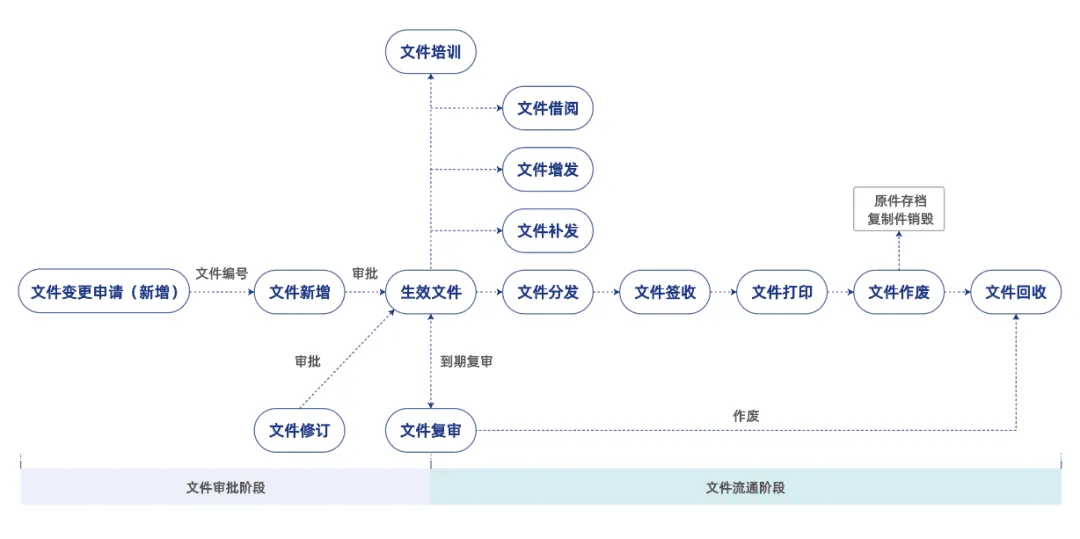
系统预设文件编号规则,申请时自动生成,杜绝重号、错号。文件任何修订均强制生成新版本,旧版本自动归档并标注“已作废”。线上唯一生效版本,彻底解决新旧文件混淆使用的致命问题。
核心解决场景二:实现“记录完整可追溯”
从文件创建、审批、发布、分发、签收、打印、借阅、回收到作废,每一步操作自动生成不可篡改的审计追踪记录。随时可查“谁、在什么时候、对什么文件、做了什么操作”,轻松应对飞检中对数据完整性的严苛拷问。
核心解决场景三:确保“流程合规高效”
自定义搭建符合企业实际的电子化审批流程。修订、复审、作废到期前系统自动提醒,避免遗漏。关联文件同步更新,变“人找事”为“事找人”,将文件管理员从繁琐的协调催促中解放出来。
核心解决场景四:筑牢“文件安全防线”
通过精密权限矩阵、动态水印、受控打印(记录唯一分发号)、操作日志监控等功能,构建文件流转全过程的安全围栏,保护企业核心知识产权与商业秘密。

睿展数据DMS不仅是一套软件,更是融合了行业最佳实践的管理方法论。我们曾助力国内高端医疗器械头部企业,成功应对数万份体系文件的数字化管理挑战,实现:
管理效率跃升:
文件检索从小时级降至秒级,审批流程周期平均缩短70%。
合规风险可控:
文件收发平衡率达成100%,版本误用风险归零,顺利通过多次国内外权威机构审计。
运营成本降低:
纸质文件打印消耗减少60%以上,文控人员得以从基础事务转向高价值数据分析。
该系统支持集团化多工厂、多子公司部署,既能实现集团统一管控,又能满足各实体个性化需求,是大型医疗器械集团实现标准化、精细化管理的得力引擎。
当监管的探照灯一次次照亮质量管理体系的暗角,文件管理的规范化已从“加分项”变为“生存项”。34家企业的名单,是警示,更是启示。
别再让宝贵的研发成果和市场声誉,湮没在文件管理的混乱与风险之中。飞检风暴之下,主动构筑数字化的合规防线,是企业最明智的战略选择。

公众号
研发中心
长沙高新区麓谷企业广场F3栋10楼
运营中心
长沙雨花区双塔国际广场B座14楼
南京办事处
南京栖霞区红枫科技园D11栋6楼
联系方式
400 900 3068
商务邮箱
market@rzdata.net
客服邮箱
support@rzdata.net


