
《国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告》中明确要求2022年6月1日起,所有三类医疗器械都应当覆盖唯一标识。此外,《医疗器械生产监督管理办法》规定:未按照法规要求执行唯一标识的企业,将罚款1万元-10万元不等。
UDI实施距离全面推行已经不远了,不少二类生产企业也开始着手UDI实施工作。不过,平台在与客户的沟通中发现,还有相当一部分企业对UDI的认知存在较大局限性,为消除认知盲区,提升企业UDI实施能力,本期特编辑了一份UDI实施规范指南,从基础知识到实施步骤、相关应用均作了梳理,方便企业更好地了解UDI体系。
01、什么是UDI?
UDI是医疗器械唯一标识(Unique Device Identification)的英文缩写,是指在医疗器械产品或包装上附载的,由数字、字母或者符号组成的代码,用于对医疗器械进行唯一性识别。完整的UDI系统包括唯一标识、数据载体和数据库(存储产品标识与关联信息)3个部分。
02、UDI在各个主体的应用
监管机构:对各级医疗器械相关企业及产品进行有效监测,控制医疗风险,减少医疗失误,提升监管效率。
生产企业:改善生产、包装和供应流程;完善产品信息化追溯和不良事件监测,实现精准召回,提升物流管控效率。
流通方(渠道商):简化分销流程,提升产品精准识别、进销存信息化管理。
使用者(医院、患者):自动识别和验证产品,加强器械采购和使用等方面的管理,减少差错;优化结算管理、与患者绑定用于临床评价,保护患者权益。
03、UDI实施的药监要求
唯一标识赋码:生产的医疗器械应当具有医疗器械唯一标识;
唯一标识注册系统提交:申请首次注册、延续注册或者注册变更时,注册申请人/注册人应当在注册管理系统中提交其最小销售单元的产品标识;
唯一标识数据库提交:在其上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库,确保数据真实、准确、完整、可追溯。
04、UDI实施流程
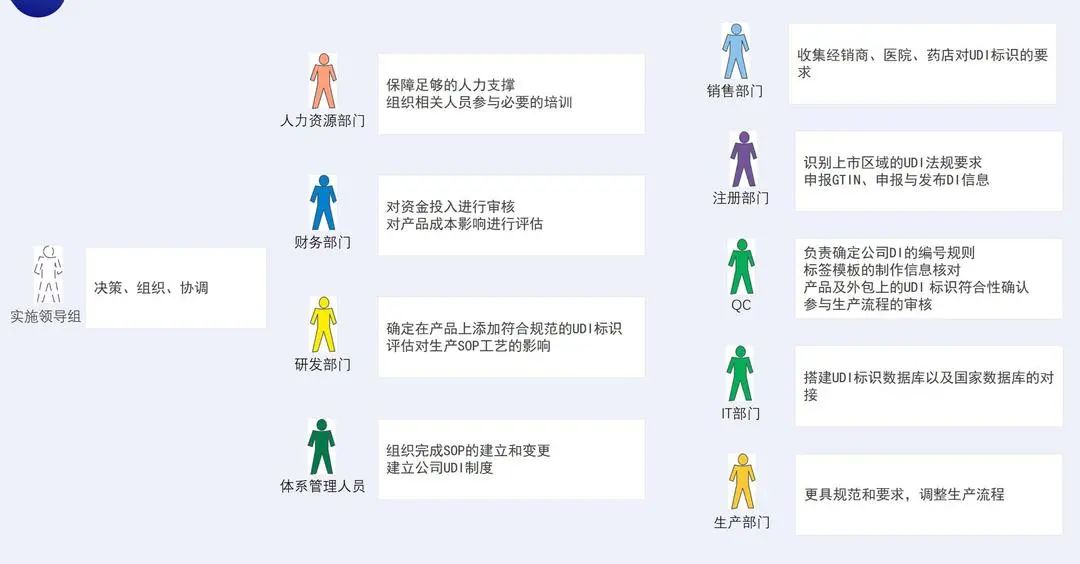
第一步,组建UDI实施团队。UDI实施是一项系统工作,涉及内容多,要求标准高,因此需要筹建研发、注册、生产等多个部门,部门之间协同联动。
第二步,学习相关法规政策。企业需要根据自己的业务范围,对中国、美国、欧盟等国家和地区的UDI实施政策进行深度学习,确保实施合规。
第三步,确定发码机构。目前国内有三家发码机构:中国物品编码中心(GS1)、中关村二维码研究院(MA码)、阿里健康(AHM码)。GS1属于全球通用的编码系统,应用最为广泛。
第四步,确定UDI编码规则。在进行UDI编码之前,企业应先确定产品的最小销售单元、包装层级和PI编码规则(生产标识动态)等,企业须遵循监管部门的要求进行编码分配。
第五步,选择UDI落地方案。这里分为三个部分:载体选择和标签设计、标签赋码、标签质量检测。
UDI载体包括一维码、二维码和射频标签。载体的标签设计应符合《医疗器械唯一标识系统规则》,满足自动识别和数据采集技术以及人工识读要求,如空间有限或者使用受限,应当有限采用符合自动识别和数据采集技术的载体形式。
目前常用的赋码方式主要分为三类:一是单独打印标签纸,然后再粘贴到产品或者盒箱上;二是直接在包装盒上喷码;三是在产品本体上刻印UDI标识,企业可根据自己的产品特性来选择赋码方式及相对应的耗材。

标签质量检测是UDI实施的重要一环,企业需确保打印的UDI标识符合质量等级的要求,否则会造成返厂、交货延期等一系列不良后果。这里建议企业选择专用的仪器进行检测,可大幅提升检测速度和有效性。
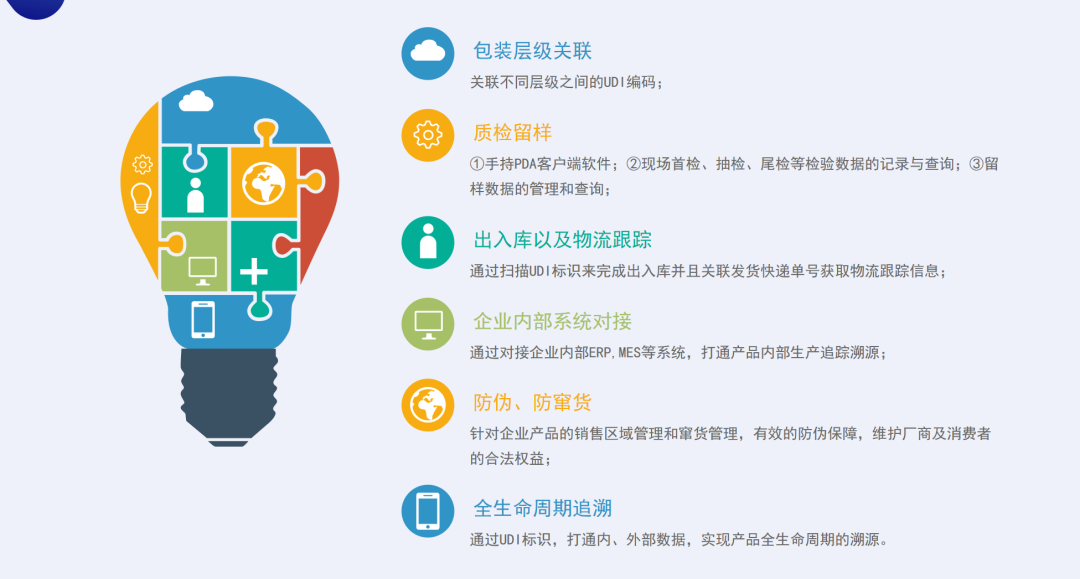
第六步,扩展UDI相关应用。企业在确定UDI落地方案后,可自行选择是否需要将UDI标识系统与内外部系统进行连接贯通,比如:包装层级关联、质检留样、出入库以及物流跟踪、企业内部系统对接、防伪防窜货、全生命周期追溯。
总而言之,UDI实施是一个系统性工程,企业在着手实施之前,需要规划好完整的实施步骤和具体实施计划,并配备好相应的人员和设施。可能有的企业会有疑问,如果公司现有的条件不足以支持整套UDI实施方案,怎么办?
那么,您可以选择一个合适的UDI实施服务商。优质的平台服务商不仅可以帮助企业规避风险、少走弯路,提高实施效率,还能有效节约成本。
睿展数据作为深耕生物医药行业数年的信息技术与数据服务解决方案提供商,在UDI实施方面已掌握相当成熟的技术,可为医疗器械企业提供基于GS1标准的UDI编码、申报、赋码、检测、数据管理、UDI生产应用、UDI追溯等一站式UDI服务,帮企业清理各类实施障碍,让UDI合规实施更高效。
想要了解更多UDI合规实施相关内容,可扫描下方二维码与张老师联系,或拨打专家热线:400-900-3068。


UDI 一站式服务平台微信公众号
研发中心
长沙高新区麓谷企业广场F3栋10楼
运营中心
长沙雨花区双塔国际广场B座14楼
南京办事处
南京栖霞区红枫科技园D11栋6楼
联系方式
400 900 3068
商务邮箱
market@rzdata.net
客服邮箱
support@rzdata.net



